為保障江蘇省醫(yī)療器械注冊人制度試點工作的順利開展��,我局制定并發(fā)布了《江蘇省醫(yī)療器械注冊人制度試點工作實施指南(試行)》(以下簡稱《指南》)?,F(xiàn)依據(jù)《指南》就企業(yè)咨詢較為集中的問題解答如下:
引言:為保障江蘇省醫(yī)療器械注冊人制度試點工作的順利開展,我局制定并發(fā)布了《江蘇省醫(yī)療器械注冊人制度試點工作實施指南(試行)》(以下簡稱《指南》)?���,F(xiàn)依據(jù)《指南》就企業(yè)咨詢較為集中的問題解答如下:

1.參與長江三角洲區(qū)域(滬蘇皖浙一市三?��。┽t(yī)療器械注冊人制度試點的委托范圍和受托范圍是什么?位于長江三角洲區(qū)域內(nèi)的醫(yī)療器械注冊申請人可以委托21個試點省份內(nèi)具備相應(yīng)生產(chǎn)能力的企業(yè)生產(chǎn)用于醫(yī)療器械注冊型式檢驗的樣品或批量生產(chǎn)擬上市銷售的醫(yī)療器械成品���。注冊人可以委托21個試點省份內(nèi)符合條件的醫(yī)療器械生產(chǎn)企業(yè)生產(chǎn)已獲證產(chǎn)品���。建議醫(yī)療器械注冊申請人或注冊人優(yōu)先選擇長江三角洲區(qū)域內(nèi)第二�����、第三類醫(yī)療器械生產(chǎn)企業(yè)進行委托生產(chǎn)����。位于長江三角洲區(qū)域內(nèi)的符合條件的企業(yè)可以接受21個試點省份內(nèi)注冊申請人或注冊人的受托生產(chǎn)。建議長江三角洲區(qū)域內(nèi)具備條件的第二�、第三類醫(yī)療器械生產(chǎn)企業(yè)積極參與全國試點范圍內(nèi)醫(yī)療器械注冊申請人或注冊人的受托生產(chǎn)。2.江蘇省醫(yī)療器械注冊人制度試點的辦理流程是怎樣的�?江蘇省注冊申請人委托21個試點省份內(nèi)具備相應(yīng)生產(chǎn)能力的企業(yè)生產(chǎn)的,首先申請醫(yī)療器械產(chǎn)品注冊�����,取得醫(yī)療器械注冊證�。然后受托生產(chǎn)企業(yè)辦理受托備案�����,取得受托生產(chǎn)備案憑證��。最后受托生產(chǎn)企業(yè)申請受托生產(chǎn)許可(開辦)或生產(chǎn)許可變更���,取得醫(yī)療器械生產(chǎn)許可證,即可進行委托生產(chǎn)���。若注冊申請人與受托生產(chǎn)企業(yè)都位于江蘇省的�,可申請或者變更申請合并檢查��。具體流程如下圖1�。
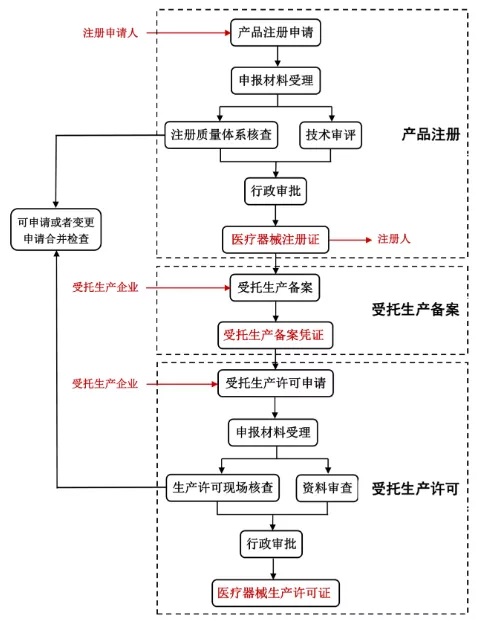
1.江蘇省醫(yī)療器械注冊人制度試點辦理流程及申報主體
注冊人已經(jīng)獲得醫(yī)療器械注冊證并需要委托生產(chǎn)的,受托生產(chǎn)企業(yè)首先辦理受托備案�����,取得受托生產(chǎn)備案憑證�。然后受托生產(chǎn)企業(yè)申請受托生產(chǎn)許可(開辦)或生產(chǎn)許可變更,取得醫(yī)療器械生產(chǎn)許可證����。最后����,注冊人申請醫(yī)療器械注冊證登記事項變更�����,取得醫(yī)療器械注冊證變更文件�。具體如下圖2。
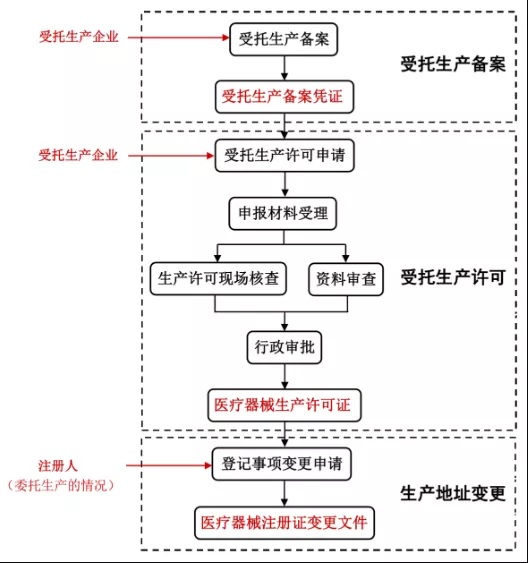
圖2.江蘇省醫(yī)療器械注冊人制度試點辦理流程及申報主體關(guān)于產(chǎn)品注冊���、生產(chǎn)許可的申報要求可以在省局網(wǎng)站政務(wù)服務(wù)——辦事指南欄目中查看���,具體網(wǎng)址如下:http://www.jszwfw.gov.cn/jszwfw/bscx/itemlist/fr_index.do?webId=1&themid=&deptid=320000SY#fw_jump不同許可事項申請表已經(jīng)上傳更新版本��,需要提交材料的請至網(wǎng)站下載并使用最新版本����,以下提供部分許可事項辦理流程和辦理材料要求的網(wǎng)址:江蘇省第二類醫(yī)療器械擬上市產(chǎn)品注冊http://www.jszwfw.gov.cn/jszwfw/bscx/itemlist/bszn.do?webId=1&iddept_yw_inf=7bff9c5195e9433e8382769aa183947a&ql_kind=01&iddept_ql_inf=433&iszx=江蘇省第二類體外診斷試劑擬上市產(chǎn)品注冊http://www.jszwfw.gov.cn/jszwfw/bscx/itemlist/bszn.do?webId=1&iddept_yw_inf=5abdda919be0429994efa59d4a79488a&ql_kind=01&iddept_ql_inf=433&iszx=開辦第二、三類醫(yī)療器械生產(chǎn)企業(yè)http://www.jszwfw.gov.cn/jszwfw/bscx/itemlist/bszn.do?webId=1&iddept_yw_inf=6948a9afa8e344edb41d69331fae7243&ql_kind=01&iddept_ql_inf=434&iszx=醫(yī)療器械生產(chǎn)許可證許可事項變更http://www.jszwfw.gov.cn/jszwfw/bscx/itemlist/bszn.do?webId=1&iddept_yw_inf=ca142901abe340a290b130f4f0a125c7&ql_kind=01&iddept_ql_inf=434&iszx=3.制度試點實施允許委托生產(chǎn)產(chǎn)品范圍包括哪些�����?制度試點實施允許委托生產(chǎn)產(chǎn)品范圍包括第二類、三類醫(yī)療器械��;屬于原國家食品藥品監(jiān)督管理總局發(fā)布的禁止委托生產(chǎn)醫(yī)療器械目錄的產(chǎn)品����,原則上不列入試點范圍。值得注意的是���,第一類醫(yī)療器械不包含在試點范圍內(nèi)��。4.注冊申請人委托生產(chǎn)的���,申報第二類醫(yī)療器械注冊時,除符合《國家食品藥品監(jiān)督管理總局關(guān)于公布醫(yī)療器械注冊申報資料要求和批準證明文件格式的公告(2014年第43號)》或《國家食品藥品監(jiān)督管理總局關(guān)于公布體外診斷試劑注冊申報資料要求和批準證明文件格式的公告(2014年第44號)》等要求外����,還需要根據(jù)《江蘇省醫(yī)療器械注冊人制度試點工作實施指南(試行)》提交哪些資料(見《指南》第四條)?(1)受托生產(chǎn)企業(yè)的營業(yè)執(zhí)照復印件���;(2)注冊申請人的質(zhì)量管理能力自查報告�;(3)委托生產(chǎn)合同復印件(明確雙方合作生產(chǎn)方式�,委托方和受托方的權(quán)利、義務(wù)與責任�����,產(chǎn)品驗收標準,產(chǎn)品損害賠償�,合同終止條件等);(4)現(xiàn)場考核評估報告(注冊申請人對受托生產(chǎn)企業(yè)的生產(chǎn)條件���、技術(shù)水平�、質(zhì)量管理情況進行現(xiàn)場考核評估�,闡述該受托企業(yè)與所合作品種的匹配性,以及合作關(guān)系確立后的定期審核計劃)��;(5)委托生產(chǎn)質(zhì)量協(xié)議復印件(明確委托生產(chǎn)的范圍��,雙方在產(chǎn)品質(zhì)量實現(xiàn)的全過程中各自的質(zhì)量安全責任�����、權(quán)利和義務(wù)�����,質(zhì)量管理體系的要求��,產(chǎn)品的性能�、生產(chǎn)、質(zhì)控要求�,委托生產(chǎn)的變更控制與審批,雙方發(fā)生分歧的解決等)�����;(6)知識產(chǎn)權(quán)保護協(xié)議復印件(明確雙方在知識產(chǎn)權(quán)保護方面各自的的責任����、權(quán)利和義務(wù));(7)轉(zhuǎn)移文件清單(例如技術(shù)要求����、生產(chǎn)工藝、原材料要求��、說明書和標簽等技術(shù)文件已有效轉(zhuǎn)移給擬受托生產(chǎn)企業(yè)����,并形成文件清單)。5.符合條件的集團公司向省局辦理內(nèi)部醫(yī)療器械注冊人變更的�����,需要根據(jù)《江蘇省醫(yī)療器械注冊人制度試點工作實施指南(試行)》提交哪些資料(見《指南》第七條)�����?(1)雙方隸屬于同一集團公司的股權(quán)證明復印件;(2)轉(zhuǎn)移文件清單(例如技術(shù)要求��、生產(chǎn)工藝���、原材料要求�、說明書和標簽等技術(shù)文件已有效轉(zhuǎn)移給擬受托生產(chǎn)企業(yè)����,并形成文件清單);(3)明確變更前已上市產(chǎn)品質(zhì)量責任主體的協(xié)議/合同復印件����;(4)承諾生產(chǎn)地址、生產(chǎn)條件和技術(shù)要求等生產(chǎn)要素不發(fā)生改變的保證聲明���;(5)對變更過程及變更后果承擔法律責任的保證聲明����,以及與集團總公司簽訂的擔保協(xié)議復印件���;(6)43號公告或44號公告中登記事項變更要求的其他資料����。以上(1)至(5)資料均需變更雙方同時簽章�����。符合要求的�,省局參照登記事項變更程序辦理。6.注冊人委托生產(chǎn)的����,受托生產(chǎn)企業(yè)需向省局辦理受托生產(chǎn)備案,備案時應(yīng)當根據(jù)《江蘇省醫(yī)療器械注冊人制度試點工作實施指南(試行)》提交哪些資料(見《指南》第十條)�����?(1)醫(yī)療器械受托生產(chǎn)備案表��;(2)受托生產(chǎn)的《醫(yī)療器械注冊證》復印件�����;(3)注冊人的營業(yè)執(zhí)照復印件����;(4)受托生產(chǎn)企業(yè)的營業(yè)執(zhí)照復印件����;(5)委托生產(chǎn)合同��;(6)委托生產(chǎn)質(zhì)量協(xié)議復印件����;(7)受托生產(chǎn)企業(yè)的《醫(yī)療器械生產(chǎn)許可證》復印件(如有);(8)受托生產(chǎn)企業(yè)具備相應(yīng)生產(chǎn)能力的證明材料(例如受托生產(chǎn)企業(yè)質(zhì)量管理體系情況證明文件)���;(9)經(jīng)辦人授權(quán)證明���。我局負責對提交的資料進行審核,評估受托生產(chǎn)企業(yè)是否具備受托生產(chǎn)條件����,比如受托生產(chǎn)企業(yè)的人員管理、生產(chǎn)廠房�����、設(shè)施設(shè)備是否與受托生產(chǎn)產(chǎn)品的生產(chǎn)規(guī)模和品種等相匹配�。7.受托生產(chǎn)企業(yè)向省局申請受托生產(chǎn)許可或生產(chǎn)許可變更的,除應(yīng)當符合省局對二�、三類醫(yī)療器械生產(chǎn)許可申報資料的要求外�����,還需要根據(jù)《江蘇省醫(yī)療器械注冊人制度試點工作實施指南(試行)》提交哪些資料(見《指南》第十一條)?(1)注冊人營業(yè)執(zhí)照復印件����;(2)受托生產(chǎn)產(chǎn)品的《醫(yī)療器械注冊證》復印件;(3)受托生產(chǎn)產(chǎn)品的產(chǎn)品技術(shù)要求復印件;(4)受托生產(chǎn)產(chǎn)品擬采用的說明書和標簽樣稿����;(5)《受托生產(chǎn)備案憑證》復印件;(6)委托生產(chǎn)合同復印件�����;(7)委托生產(chǎn)質(zhì)量協(xié)議復印件���;(8)知識產(chǎn)權(quán)保護協(xié)議復印件��。8.注冊申請人委托生產(chǎn)的���,注冊質(zhì)量管理體系核查范圍還包括哪些方面?注冊申請人委托生產(chǎn)的,原則上應(yīng)當對注冊申請人及受托生產(chǎn)企業(yè)的質(zhì)量管理體系同步進行現(xiàn)場核查��。注冊質(zhì)量管理體系核查范圍還包含以下幾種情況:(1)同一注冊申請人委托多家企業(yè)生產(chǎn)的,應(yīng)當對注冊申請人以及相關(guān)受托生產(chǎn)企業(yè)進行現(xiàn)場核查���;(2)注冊申請人僅為樣品研發(fā)主體�,生產(chǎn)工藝建立和驗證�、設(shè)計轉(zhuǎn)換均在受托生產(chǎn)企業(yè)完成的,應(yīng)當對注冊申請人研發(fā)地址和受托企業(yè)生產(chǎn)地址進行同步核查�;(3)注冊申請人委托外部機構(gòu)進行設(shè)計開發(fā)的,注冊體系核查可以根據(jù)情況對受托研發(fā)企業(yè)進行延伸核查����。(4)根據(jù)受托生產(chǎn)企業(yè)情況對關(guān)鍵物料或者關(guān)鍵工序/特殊過程的供應(yīng)商進行延伸核查。(5)注冊申請人委托本省內(nèi)企業(yè)生產(chǎn)的�,注冊質(zhì)量管理體系現(xiàn)場核查可與生產(chǎn)許可申請或者變更申請合并檢查。9. 注冊申請人委托生產(chǎn)的���,注冊質(zhì)量管理體系核查除需按照《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》要求外�,還需重點關(guān)注哪些方面�?對于參與試點的醫(yī)療器械注冊申請人和受托生產(chǎn)企業(yè)在體系核查重點上與原來有所區(qū)別:(1)注冊申請人具備承擔醫(yī)療器械質(zhì)量安全責任的能力;(2)注冊申請人對受托生產(chǎn)企業(yè)進行質(zhì)量管理體系評估���、審核和監(jiān)督的能力��;(3)注冊申請人對委托生產(chǎn)產(chǎn)品的技術(shù)文件����、生產(chǎn)工藝、設(shè)計變更等有效轉(zhuǎn)移情況��;(4)注冊申請人所選擇的受托生產(chǎn)企業(yè)具有持續(xù)穩(wěn)定生產(chǎn)合格受托產(chǎn)品的能力�。10.注冊人委托生產(chǎn)的���,生產(chǎn)許可現(xiàn)場核查除需按照《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》要求外�����,還需重點關(guān)注哪些方面?對于參與試點的受托生產(chǎn)企業(yè)在現(xiàn)場核查重點上與原來有所區(qū)別:(1)受托生產(chǎn)企業(yè)應(yīng)當具備與擬生產(chǎn)醫(yī)療器械相適應(yīng)的質(zhì)量管理體系及相應(yīng)人員配備和管理經(jīng)驗�;(2)受托生產(chǎn)企業(yè)應(yīng)當具備與產(chǎn)品相適應(yīng)的生產(chǎn)廠房���、設(shè)備設(shè)施�、質(zhì)量檢驗設(shè)施及同類產(chǎn)品生產(chǎn)經(jīng)驗等��;(3)受托生產(chǎn)企業(yè)對受托品種生產(chǎn)工藝流程����、原材料要求等的理解和控制情況;(4)受托生產(chǎn)企業(yè)對共線生產(chǎn)的可行性評估和執(zhí)行情況(受托產(chǎn)品與原有產(chǎn)品為共線生產(chǎn)的情況適用);(5)受托生產(chǎn)企業(yè)是否具備接受多個注冊人委托生產(chǎn)的能力(同時接受多個注冊人委托生產(chǎn)的情況適用)��。