《醫(yī)療器械生產(chǎn)監(jiān)督管理辦法》的規(guī)定�����,開辦第二類��、第三類醫(yī)療器械生產(chǎn)企業(yè)的���,應(yīng)當向所在地省�����、自治區(qū)��、直轄市藥品監(jiān)督管理部門申請生產(chǎn)許可����,第一類醫(yī)療器械生產(chǎn)企業(yè)辦理備案�����。在此為大家講解三類醫(yī)療器械注冊流程和要求。
引言:《醫(yī)療器械生產(chǎn)監(jiān)督管理辦法》的規(guī)定�����,開辦第二類���、第三類醫(yī)療器械生產(chǎn)企業(yè)的���,應(yīng)當向所在地省、自治區(qū)��、直轄市藥品監(jiān)督管理部門申請生產(chǎn)許可�,第一類醫(yī)療器械生產(chǎn)企業(yè)辦理備案����。在此為大家講解三類醫(yī)療器械注冊流程和要求。
一���、三類醫(yī)療器械注冊向哪里申報:
國家規(guī)定�����,三類醫(yī)療器械注冊由國家局受理和審批���;二類醫(yī)療器械有各省藥監(jiān)局受理并審批�����。PS:從各種渠道已有消息透出�����,二類醫(yī)療器械的注冊未來可能由國家局受理�、審批���,但暫未看到明文的政策發(fā)布�。
二�、三類醫(yī)療器械注冊一般流程:
三類醫(yī)療器械注冊流程如下:
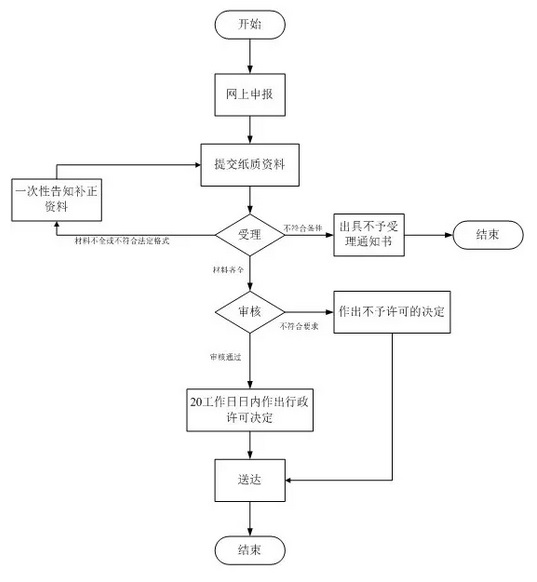
三、三類醫(yī)療器械注冊申報資料:
(一)《醫(yī)療器械生產(chǎn)企業(yè)開辦申請表》(原件)(包含委托書及被委托人身份證復(fù)印件, 以及申請材料真實性的保證聲明)���。
(二)營業(yè)執(zhí)照復(fù)印件��。
(三)申請企業(yè)持有的所生產(chǎn)醫(yī)療器械注冊證及產(chǎn)品技術(shù)要求復(fù)印件�����。
(四)法定代表人�����、企業(yè)負責(zé)人身份證明復(fù)印件��;企業(yè)負責(zé)人任命文件的復(fù)印件����;生產(chǎn)管理、質(zhì)量檢驗崗位從業(yè)人員學(xué)歷��、職稱一覽表�。
(五)生產(chǎn)、質(zhì)量和技術(shù)部門負責(zé)人的身份����、學(xué)歷���、職稱證明和工作簡歷(復(fù)印件)�����。
(六)擬生產(chǎn)產(chǎn)品范圍�����、品種和相關(guān)產(chǎn)品簡介(產(chǎn)品簡介至少包括對產(chǎn)品的結(jié)構(gòu)組成��、原理����、預(yù)期用途的說明及產(chǎn)品標準)。
(七)生產(chǎn)場地的證明文件�����,有特殊生產(chǎn)環(huán)境要求的還應(yīng)當提交設(shè)施�����、環(huán)境的證明文件復(fù)印件��;一般包含房屋產(chǎn)權(quán)證明或租賃協(xié)議及出租方房產(chǎn)證明復(fù)印件�����、廠區(qū)總平面圖����、主要生產(chǎn)車間平面圖�。
(八)主要生產(chǎn)設(shè)備和檢驗儀器清單(原件)����。
(九)質(zhì)量手冊和程序文件(原件)。
(十)工藝流程圖(原件)��。
(十一)生產(chǎn)企業(yè)自查表(原件)�����。
(十二)其他證明資料����。
注:其他依據(jù)各地藥監(jiān)局的具體規(guī)定準備。
四��、醫(yī)療器械生產(chǎn)許可證圖示:

杭州證標客醫(yī)藥技術(shù)咨詢有限公司位于中國杭州�,是醫(yī)療器械專業(yè)服務(wù)第三方。為廣大客戶提供醫(yī)療器械法律法規(guī)����、經(jīng)營開辦��、醫(yī)療器械生產(chǎn)質(zhì)量管理體系、醫(yī)療器械注冊�����、臨床�、CRC、CE��、FDA���、醫(yī)療信息系統(tǒng)定制開發(fā)一站式服務(wù)��,是江浙滬地區(qū)極少數(shù)有醫(yī)療器械全流程服務(wù)能力的機構(gòu)之一���。任何有關(guān)醫(yī)療器械注冊、醫(yī)療器械經(jīng)營許可/備案�、醫(yī)療器械臨床試驗、CRC服務(wù)事宜���,隨時方便聯(lián)系葉工(MP:18058734169��,微信同)���。