2023年4月28日����,國(guó)家藥監(jiān)局發(fā)布《應(yīng)用納米材料的醫(yī)療器械安全性和有效性評(píng)價(jià)指導(dǎo)原則第二部分:理化表征》,本指導(dǎo)原則為注冊(cè)申請(qǐng)人/監(jiān)管人員提供關(guān)于應(yīng)用納米材料的醫(yī)療器械理化表征相關(guān)方面的信息�。本指導(dǎo)原則是對(duì)應(yīng)用納米材料醫(yī)療器械理化表征的一般要求,醫(yī)療器械注冊(cè)申請(qǐng)人應(yīng)依據(jù)具體產(chǎn)品的特性對(duì)注冊(cè)申報(bào)資料的內(nèi)容進(jìn)行充分說(shuō)明和細(xì)化�。
應(yīng)用納米材料的醫(yī)療器械安全性和有效性評(píng)價(jià)指導(dǎo)原則第二部分:理化表征
本指導(dǎo)原則為注冊(cè)申請(qǐng)人/監(jiān)管人員提供關(guān)于應(yīng)用納米材料的醫(yī)療器械理化表征相關(guān)方面的信息。
本指導(dǎo)原則是對(duì)應(yīng)用納米材料醫(yī)療器械理化表征的一般要求�,醫(yī)療器械注冊(cè)申請(qǐng)人應(yīng)依據(jù)具體產(chǎn)品的特性對(duì)注冊(cè)申報(bào)資料的內(nèi)容進(jìn)行充分說(shuō)明和細(xì)化。注冊(cè)申請(qǐng)人還應(yīng)依據(jù)具體產(chǎn)品的特性確定其中的相關(guān)內(nèi)容是否適用����,若不適用�,需詳細(xì)闡述理由及相應(yīng)的科學(xué)依據(jù)。
本指導(dǎo)原則是對(duì)醫(yī)療器械注冊(cè)申請(qǐng)人和審評(píng)人員的指導(dǎo)性文件���,但不包括注冊(cè)審批所涉及的行政事項(xiàng)����,亦不作為法規(guī)強(qiáng)制執(zhí)行�����,如果有能滿足相關(guān)法規(guī)要求的其它方法,也可以采用�����,但是需要提供詳細(xì)的研究資料和驗(yàn)證資料�����。應(yīng)在遵循相關(guān)法規(guī)的前提下使用本指導(dǎo)原則��。
本指導(dǎo)原則是在現(xiàn)行法規(guī)和標(biāo)準(zhǔn)體系以及當(dāng)前認(rèn)知水平下制定的�,隨著法規(guī)和標(biāo)準(zhǔn)的不斷完善,以及科學(xué)技術(shù)的不斷發(fā)展�,本指導(dǎo)原則相關(guān)內(nèi)容也將進(jìn)行適時(shí)的調(diào)整。
一�、適用范圍
本指導(dǎo)原則適用于與人體直接或間接接觸,由納米材料組成或包含納米材料的醫(yī)療器械的理化表征��。
不適用于:
- 應(yīng)用納米材料的體外診斷產(chǎn)品�����;
- 應(yīng)用納米材料的藥品�;
- 納米技術(shù)賦能的醫(yī)療產(chǎn)品(如納米機(jī)器人);
- 應(yīng)用納米材料的醫(yī)療器械在制造和廢棄過(guò)程中造成的職業(yè)和環(huán)境風(fēng)險(xiǎn)�。
二��、理化表征在應(yīng)用納米材料的醫(yī)療器械申報(bào)資料中的體現(xiàn)
應(yīng)用納米材料的醫(yī)療器械產(chǎn)品的安全性和有效性與所使用的納米材料的理化性質(zhì)(如化學(xué)組成��、尺寸及尺寸分布����、形態(tài)學(xué)�����、表面特性等)緊密相關(guān)���。根據(jù)國(guó)家藥品監(jiān)督管理局發(fā)布的《關(guān)于公布醫(yī)療器械注冊(cè)申報(bào)資料要求和批準(zhǔn)證明文件格式的公告》����,理化表征在應(yīng)用納米材料的醫(yī)療器械產(chǎn)品安全性和有效性評(píng)價(jià)的意義和作用主要體現(xiàn)在以下申報(bào)資料中:
(一)監(jiān)管信息(委托信息��、主文檔授權(quán)信)
應(yīng)用納米材料的醫(yī)療器械產(chǎn)品注冊(cè)申請(qǐng)人可自行獨(dú)立研發(fā)���、或委托第三方研發(fā)納米原材料,或直接外購(gòu)納米原材料����。注冊(cè)申請(qǐng)人應(yīng)具備對(duì)于納米原材料的完整評(píng)價(jià)和供應(yīng)商審核能力,并證明其對(duì)醫(yī)療器械終產(chǎn)品生產(chǎn)關(guān)鍵工藝及參數(shù)進(jìn)行質(zhì)量控制的能力。因此���,如果醫(yī)療器械的原材料為納米材料�,注冊(cè)申請(qǐng)人應(yīng)提供包括納米原材料的理化表征在內(nèi)的質(zhì)量控制文件��。如果委托其他企業(yè)生產(chǎn)的����,應(yīng)當(dāng)提供受托企業(yè)資格文件、委托合同和質(zhì)量協(xié)議����。在質(zhì)量協(xié)議中,應(yīng)提供納米材料質(zhì)量控制相關(guān)參數(shù)�。如果原材料供應(yīng)商已在國(guó)家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評(píng)中心進(jìn)行過(guò)主文檔備案,應(yīng)提交主文檔授權(quán)信��。
(二)研究資料(產(chǎn)品化學(xué)和物理性能研究)
注冊(cè)申請(qǐng)人在設(shè)計(jì)應(yīng)用納米材料的醫(yī)療器械時(shí)�����,預(yù)期利用納米材料的某些特殊性能�����,如小尺寸、高比表面積���、高化學(xué)活性�����,或者利用納米表面特性對(duì)于體內(nèi)微環(huán)境的影響來(lái)發(fā)揮其功能���。如納米銀敷料利用了納米銀在一定時(shí)期內(nèi)可持續(xù)釋放銀的特性。又如某些骨科植入物表面納米結(jié)構(gòu)的設(shè)計(jì)�����,可以促進(jìn)骨重建過(guò)程��。為證明產(chǎn)品中所設(shè)計(jì)應(yīng)用的納米材料能夠發(fā)揮預(yù)期特性�����,注冊(cè)申請(qǐng)人需開(kāi)展有針對(duì)性的理化性質(zhì)表征���。這些研究也將成為確定產(chǎn)品技術(shù)要求中科學(xué)合理的性能指標(biāo)和檢驗(yàn)方法的關(guān)鍵依據(jù)。
(三)研究資料(產(chǎn)品生物學(xué)特性研究)
現(xiàn)行的GB/T 16886.1(ISO 10993.1)將理化表征作為醫(yī)療器械生物相容性評(píng)價(jià)的起點(diǎn)���。對(duì)于應(yīng)用納米材料的醫(yī)療器械����,這一點(diǎn)尤為重要,因納米材料的生物學(xué)效應(yīng)取決于其理化性質(zhì)�,如尺寸及尺寸分布、形態(tài)學(xué)�、表面特性、化學(xué)組成��、團(tuán)聚/聚集狀態(tài)等�。在生物相容性/毒理學(xué)研究過(guò)程中,注冊(cè)申請(qǐng)人不僅要對(duì)醫(yī)療器械產(chǎn)品中的納米材料開(kāi)展理化表征�,而且根據(jù)風(fēng)險(xiǎn)分析,確定是否需要針對(duì)在生物組織/體液中的納米材料及其代謝/轉(zhuǎn)歸產(chǎn)物開(kāi)展理化表征����。客觀���、真實(shí)的定性/定量理化表征結(jié)果�����,可為開(kāi)展生物相容性/毒理學(xué)研究提供必要的信息���。相反���,非客觀、真實(shí)的定性/定量理化表征結(jié)果���,可能導(dǎo)致對(duì)于產(chǎn)品安全性風(fēng)險(xiǎn)的錯(cuò)誤判定����。
(四)研究資料(清潔���、消毒��、滅菌研究)
在應(yīng)用納米材料的醫(yī)療器械生產(chǎn)工藝過(guò)程中�����,作為原材料之一的納米材料通常經(jīng)過(guò)多道工藝過(guò)程����,生產(chǎn)工藝過(guò)程對(duì)于終產(chǎn)品中納米材料存在狀態(tài)的影響�����,以及產(chǎn)品的批間/批內(nèi)穩(wěn)定性和均一性需要通過(guò)充分的理化表征來(lái)證明�。
建議注冊(cè)申請(qǐng)人在滅菌方法驗(yàn)證中對(duì)于納米材料特性加以考慮,如:輻照劑量對(duì)于納米材料是否存在影響����,環(huán)氧乙烷是否會(huì)殘留在納米材料結(jié)構(gòu)中難以解析等。此外����,注冊(cè)申請(qǐng)人在考慮對(duì)于驗(yàn)證所需產(chǎn)品批次和樣本量的要求時(shí),也需要通過(guò)理化表征對(duì)于納米材料在醫(yī)療器械中分布的均勻性等因素進(jìn)行研究分析��。
(五)研究資料(穩(wěn)定性研究)
理化表征同樣對(duì)于產(chǎn)品貨架有效期和包裝驗(yàn)證非常重要����。目前,產(chǎn)品有效期驗(yàn)證所采用的加速老化計(jì)算依據(jù)仍是根據(jù)傳統(tǒng)高分子材料總結(jié)的阿累尼烏斯(Arrhenius)反應(yīng)公式���,該公式是否適用于納米材料仍有待深入研究��。因此��,建議注冊(cè)申請(qǐng)人在有效期各時(shí)間點(diǎn)應(yīng)針對(duì)納米材料開(kāi)展適宜的理化表征�,以證明醫(yī)療器械中的納米材料是否在儲(chǔ)存期內(nèi)發(fā)生物理性質(zhì)和化學(xué)性質(zhì)的變化��。
(六)產(chǎn)品臨床評(píng)價(jià)資料
目前,應(yīng)用納米材料的醫(yī)療器械臨床評(píng)價(jià)尚缺乏相應(yīng)的指導(dǎo)原則/審評(píng)要點(diǎn)��。注冊(cè)申請(qǐng)人應(yīng)根據(jù)申報(bào)產(chǎn)品的適用范圍��、技術(shù)特征����、已有臨床數(shù)據(jù)等具體情況,選擇恰當(dāng)?shù)呐R床評(píng)價(jià)路徑���,包括“同品種臨床評(píng)價(jià)路徑”和/或“臨床試驗(yàn)路徑”��。若注冊(cè)申請(qǐng)人通過(guò)同品種臨床評(píng)價(jià)路徑進(jìn)行臨床評(píng)價(jià)�,除了提交申報(bào)產(chǎn)品與同品種醫(yī)療器械在適用范圍�����、技術(shù)特征��、生物學(xué)特性方面的對(duì)比資料����,注冊(cè)申請(qǐng)人還需開(kāi)展具有針對(duì)性和特異性的完整而全面的理化表征研究,這對(duì)于確定對(duì)照產(chǎn)品是否為同品種產(chǎn)品是至關(guān)重要的。
三��、納米材料理化性質(zhì)表征的基本原則
納米材料尺寸小��、比表面積大��、化學(xué)活性高�,在不同環(huán)境中表面特性和聚集狀態(tài)易發(fā)生變化�,這給納米材料的生物學(xué)效應(yīng)評(píng)估帶來(lái)挑戰(zhàn)。針對(duì)應(yīng)用納米材料的醫(yī)療器械開(kāi)展全面而準(zhǔn)確的理化性質(zhì)表征以及使用過(guò)程中納米材料理化性質(zhì)變化測(cè)量都至關(guān)重要�。應(yīng)用納米材料的醫(yī)療器械的理化表征流程圖可以參考圖1a。根據(jù)產(chǎn)品及納米材料的性質(zhì)�,可以選擇不同階段的理化檢測(cè)項(xiàng)目,流程圖1b中給出了檢測(cè)項(xiàng)目示例����。該理化表征可分為三個(gè)層次:納米原材料、醫(yī)療器械終產(chǎn)品中的納米材料���、生物組織樣本中的納米材料(僅適用于生物組織吸收了應(yīng)用納米材料的醫(yī)療器械釋放的納米材料���;或者應(yīng)用納米材料的醫(yī)療器械中的納米材料釋放并遷移到了生物組織樣本中)。
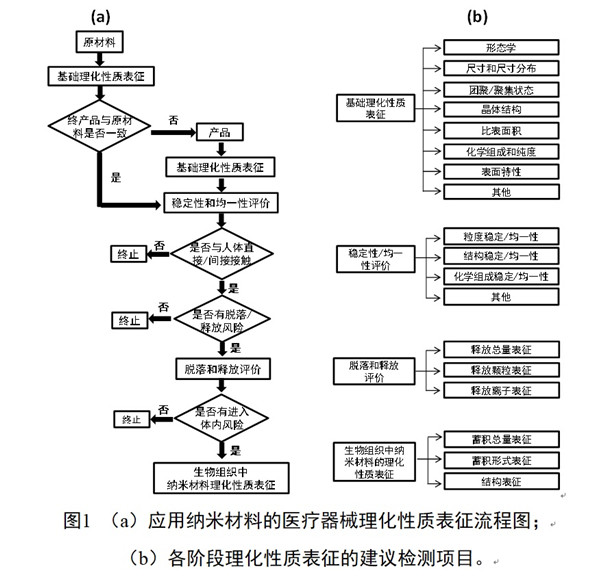
開(kāi)展應(yīng)用納米材料醫(yī)療器械理化表征的第一步是對(duì)作為醫(yī)療器械生產(chǎn)的起始納米原材料和終產(chǎn)品中的納米材料進(jìn)行理化表征����,包括形態(tài)學(xué)��、尺寸��、團(tuán)聚/聚集狀態(tài)��、晶體結(jié)構(gòu)��、比表面積����、化學(xué)組成與純度�、表面特性等。通過(guò)同時(shí)表征的數(shù)據(jù)證明起始原料的表征數(shù)據(jù)與終產(chǎn)品中應(yīng)用的納米材料是否相同��。如果相同或者有數(shù)據(jù)闡明相似的材料具有足夠相似的理化性質(zhì)��,可以考慮采用這些數(shù)據(jù)來(lái)進(jìn)行產(chǎn)品的風(fēng)險(xiǎn)評(píng)估�。如果不同,則應(yīng)以終產(chǎn)品的詳細(xì)表征數(shù)據(jù)為基礎(chǔ)進(jìn)行風(fēng)險(xiǎn)評(píng)估�����。為了確保在同一工藝參數(shù)下�,產(chǎn)品的質(zhì)量差異在可接受的偏差范圍內(nèi)����,注冊(cè)申請(qǐng)人需對(duì)產(chǎn)品中的納米材料進(jìn)行明確的穩(wěn)定性和均一性評(píng)價(jià)���。評(píng)價(jià)內(nèi)容包括儲(chǔ)存�、運(yùn)輸��、使用等過(guò)程中���,納米材料受環(huán)境等因素影響,隨時(shí)間推移造成的幾何形態(tài)學(xué)�����、尺寸�����、聚集狀態(tài)����、化學(xué)成分、氧化狀態(tài)等理化性質(zhì)的變化����。
需要強(qiáng)調(diào)的是�,納米材料可能在加工過(guò)程中改變其表面化學(xué)���,比如獲得新的或額外的表面分子��,作用類(lèi)似于涂層����;或者氧化狀態(tài)改變等����。鑒于這些潛在的表面改變,如有必要���,注冊(cè)申請(qǐng)人應(yīng)考慮納米材料在測(cè)試和/或使用的不同階段開(kāi)展理化性質(zhì)表征���。
對(duì)于與人體有直接或間接接觸的醫(yī)療器械,納米材料的脫落和釋放風(fēng)險(xiǎn)是必須要考慮的����。游離的納米材料或釋放的離子進(jìn)入體內(nèi)是可能引起在個(gè)體水平、組織水平以及細(xì)胞和分子水平上不良反應(yīng)的關(guān)鍵因素�。因此需要根據(jù)納米材料脫落/釋放的風(fēng)險(xiǎn)評(píng)估�����,對(duì)可能暴露的納米材料進(jìn)行分析與理化表征����,包括測(cè)量釋放元素的種類(lèi)與釋放元素總量�����,以及測(cè)量釋放液中可能存在的納米顆粒以及離子濃度�����。需要指出的是:納米材料的脫落和釋放評(píng)價(jià)不僅限于體外評(píng)價(jià)����,如適用���,鼓勵(lì)注冊(cè)申請(qǐng)人同時(shí)開(kāi)展體外和體內(nèi)納米材料脫落和釋放評(píng)價(jià)研究�,并將體外和體內(nèi)研究結(jié)果相關(guān)聯(lián)�����。
產(chǎn)品使用過(guò)程中脫落或釋放的納米材料,以及由納米材料釋放的離子可隨血液系統(tǒng)或淋巴系統(tǒng)進(jìn)入體內(nèi)循環(huán)��,并在組織器官中蓄積�。納米材料在生物組織中的蓄積量、存在形式(顆?����;蚱浣到猱a(chǎn)物)以及材料結(jié)構(gòu)是否出現(xiàn)缺陷決定了其在體內(nèi)的穩(wěn)定性和潛在的生物安全性��。因而如果從產(chǎn)品中脫落/釋放的納米材料有進(jìn)入體內(nèi)循環(huán)系統(tǒng)的風(fēng)險(xiǎn)��,則有必要提供生物組織中納米材料的蓄積量數(shù)據(jù)���,并證實(shí)其存在形式���、結(jié)構(gòu)等理化性質(zhì)。
如本指導(dǎo)原則第二部分所述�,在原材料質(zhì)控、產(chǎn)品有效性研究����、產(chǎn)品安全性研究、產(chǎn)品生產(chǎn)工藝和質(zhì)量控制研究�����,以及產(chǎn)品臨床評(píng)價(jià)中,需要針對(duì)不同樣本中的納米材料進(jìn)行適宜的理化表征����。注冊(cè)申請(qǐng)人、科研人員�、檢測(cè)人員,以及審評(píng)人員應(yīng)當(dāng)認(rèn)識(shí)到�����,只有采用適合產(chǎn)品特點(diǎn)����,并能最大限度保持或模擬產(chǎn)品與人體接觸暴露環(huán)境的理化表征手段,且試驗(yàn)人員和評(píng)價(jià)人員具備足夠的納米材料相關(guān)知識(shí)的前提下��,理化表征結(jié)果才能用于正確評(píng)價(jià)應(yīng)用納米材料的醫(yī)療器械安全性和有效性��。
例如�,在開(kāi)展納米銀敷料類(lèi)產(chǎn)品理化表征時(shí)���,應(yīng)在總銀含量和可溶性銀含量的測(cè)定研究中�,正確區(qū)分離子形式的銀和納米顆粒狀態(tài)的銀,同時(shí)需要區(qū)分銀的價(jià)態(tài)����。目前,測(cè)定總銀含量的主流方法是經(jīng)硝酸消解后采用ICP-MS方法分析����。注冊(cè)申請(qǐng)人應(yīng)考慮將經(jīng)驗(yàn)證的單顆粒ICP-MS、同步輻射方法�����、光電子能譜(XPS)�、高光譜成像方法等,用于實(shí)際納米銀敷料產(chǎn)品的研究����,以便區(qū)分釋放的銀是離子狀態(tài)還是顆粒狀態(tài),以及銀的價(jià)態(tài)���,同時(shí)借助原位��、無(wú)損�、高靈敏度的分析方法來(lái)明確生物轉(zhuǎn)運(yùn)過(guò)程中銀的化學(xué)性質(zhì)轉(zhuǎn)化,探討生物體銀的化學(xué)性質(zhì)信息與生物效應(yīng)的關(guān)系��。
前期研究工作已證實(shí)納米材料有可能與蛋白質(zhì)相互作用�,形成蛋白冠,影響納米顆粒的各種生物學(xué)效應(yīng)���。在銀的釋放試驗(yàn)中�����,如果僅采用簡(jiǎn)單體外模型�����,例如采用不含蛋白的純水�����、PBS或生理鹽水研究銀的釋放/溶出�����,則無(wú)法反映臨床使用中實(shí)際創(chuàng)面及其滲出液存在蛋白或其他成分的復(fù)雜情況�����,特別是形成蛋白冠現(xiàn)象�����,應(yīng)考慮這一因素對(duì)于產(chǎn)品中銀的釋放/溶出���,以及進(jìn)入體內(nèi)的行為和生物學(xué)效應(yīng)的影響。
應(yīng)用納米材料的醫(yī)療器械理化表征和測(cè)量方法示例見(jiàn)附件1的表1�����,該表內(nèi)容主要來(lái)源于GB/T 39261(ISO/TR 13014)�����,以及ISO/TR 10993.22�����。注冊(cè)申請(qǐng)人應(yīng)根據(jù)產(chǎn)品及納米材料特性選擇適合的理化表征方法組合��。此外��,如有必要�,注冊(cè)申請(qǐng)人也應(yīng)提供該表之外檢測(cè)方法獲得的額外信息以便進(jìn)行風(fēng)險(xiǎn)評(píng)估。需要指出的是,當(dāng)前大多數(shù)納米材料理化表征方法是針對(duì)科研或工業(yè)中應(yīng)用的納米材料制訂的���,并未采用實(shí)際醫(yī)療器械產(chǎn)品進(jìn)行過(guò)納米材料表征或者生物樣本中納米材料表征的驗(yàn)證和優(yōu)化����。因此��,注冊(cè)申請(qǐng)人在采用相關(guān)標(biāo)準(zhǔn)方法開(kāi)展理化表征研究時(shí)���,需對(duì)所采用的方法是否適用于應(yīng)用納米材料的醫(yī)療器械進(jìn)行驗(yàn)證�����,充分考慮所采用的方法中不適用部分的改進(jìn)和優(yōu)化����。
四�����、現(xiàn)行可用標(biāo)準(zhǔn)簡(jiǎn)介
目前���,針對(duì)納米材料或納米技術(shù)的國(guó)內(nèi)標(biāo)準(zhǔn)(包括國(guó)家標(biāo)準(zhǔn)���、行業(yè)標(biāo)準(zhǔn)、地方標(biāo)準(zhǔn)���、團(tuán)體標(biāo)準(zhǔn))有近200個(gè)���。其中涉及理化表征的技術(shù)方法類(lèi)或指南類(lèi)標(biāo)準(zhǔn)約有100個(gè),均可選擇性地被用于應(yīng)用納米材料的醫(yī)療器械理化表征檢測(cè)�����。另外����,還有很多并非針對(duì)納米材料或納米技術(shù)的方法標(biāo)準(zhǔn)也可用于應(yīng)用納米材料的醫(yī)療器械理化表征檢測(cè)。附件1的表1中盡可能收集了納米材料理化表征相關(guān)的標(biāo)準(zhǔn)��。但注冊(cè)申請(qǐng)人���、檢測(cè)機(jī)構(gòu)�����,以及審評(píng)部門(mén)應(yīng)根據(jù)應(yīng)用納米材料的醫(yī)療器械預(yù)期用途�、結(jié)構(gòu)組成、作用機(jī)理��、與人體的暴露途徑/時(shí)間����、納米材料在醫(yī)療器械中的存在形式等因素,綜合考慮上述標(biāo)準(zhǔn)是否適用于醫(yī)療器械中的納米材料表征��。
目前���,國(guó)家藥監(jiān)局已發(fā)布了三項(xiàng)專(zhuān)門(mén)針對(duì)應(yīng)用納米材料的醫(yī)療器械行業(yè)標(biāo)準(zhǔn)�,分別是YY/T 1295《醫(yī)療器械生物學(xué)評(píng)價(jià) 納米材料:細(xì)菌內(nèi)毒素試驗(yàn)》�、YY/T 0993《醫(yī)療器械生物學(xué)評(píng)價(jià) 納米材料:體外細(xì)胞毒性試驗(yàn)(MTT試驗(yàn)和LDH試驗(yàn))》,以及YY/T 1532《醫(yī)療器械生物學(xué)評(píng)價(jià) 納米材料 溶血試驗(yàn)》��,其中都涉及到對(duì)于納米材料理化表征的相關(guān)要求����。YY/T 1863《納米醫(yī)療器械生物學(xué)評(píng)價(jià) 含納米銀敷料中銀顆粒和銀離子的釋放與表征方法》行業(yè)標(biāo)準(zhǔn)即將發(fā)布,該標(biāo)準(zhǔn)給出了具體的釋放試驗(yàn)方法與表征方法�。
此外,已發(fā)布的GB/T 38261《納米技術(shù) 生物樣品中銀含量測(cè)量 電感耦合等離子體質(zhì)譜法》標(biāo)準(zhǔn)適用于各種生物組織中銀含量的定量測(cè)量��。
五���、縮略語(yǔ)和術(shù)語(yǔ)表
縮略語(yǔ)/術(shù)語(yǔ) | 英文全稱(chēng) | 解釋 |
AES | auger electron spectroscopy | 俄歇電子能譜法 |
AFM | atomic force microscopy | 原子力顯微鏡法 |
AUC | analytical ultracentrifugation | 分析型超速離心 |
BET | Brunner?Emmet?Teller method | 比表面積測(cè)量:旨在解釋氣體分子在固體表面的物理吸附的布魯諾-艾默特-泰勒(BET)理論 |
CLS | centrifugal liquid sedimentation | 液體離心沉降 |
DLS | dynamic light scattering | 動(dòng)態(tài)光散射是在一個(gè)系綜中測(cè)量顆粒粒徑分布的方法 |
DMA | differential mobility analysis | 微分遷移率分析 |
EDS | energy dispersive X-ray spectroscopy | 能量色散X射線光譜�����,可分析小至幾納米直徑的顆粒 |
EELS | electron energy loss spectroscopy | 電子能量損失譜����,可分析小至幾納米直徑的顆粒 |
EFSA | European Food Safety Authority | 歐洲食品安全局 |
ESEM | environmental scanning electron microscopy | 環(huán)境掃描電子顯微鏡法 |
FTIR | Fourier transform infrared spectroscopy | 傅里葉變換紅外光譜法 |
IR | infrared absorption spectrum | 紅外吸收光譜 |
ICP-MS | inductively coupled plasma mass spectrometry | 電感耦合等離子體質(zhì)譜法 |
ICP-OES | inductively coupled plasma-optical emission spectrometry | 電感耦合等離子體發(fā)射光譜法 |
LII | laser induced incandescence | 激光誘導(dǎo)白熾光 |
MFS | molecular fluorescence spectroscopy | 分子熒光光譜 |
MS | mass spectrometry | 質(zhì)譜法 |
NMR | nuclear magnetic resonance | 核磁共振 |
PTA | particle tracking analysis | 顆粒跟蹤分析 |
SAXS | small angle X-ray scattering | 小角X射線散射 |
SCCS | Scientific Committee on Consumer Safety | 消費(fèi)者安全科學(xué)委員會(huì) |
SEC | size exclusion chromatography | 尺寸排阻色譜 |
SEM | scanning electron microscope | 掃描電子顯微鏡法 |
SIMS | secondary ion mass spectrometry | 二次離子質(zhì)譜法 |
spICP-MS | single particle inductively coupled plasma mass spectrometry | 單顆粒電感耦合等離子體質(zhì)譜法 |
SPM | scanning probe microscopy | 掃描探針顯微鏡法 |
STM | scanning tunneling microscopy | 掃描隧道顯微鏡法 |
TEM | transmission electron microscopy | 透射電子顯微鏡法 |
TG | thermogravimetric analysis | 熱重分析 |
USAXS | ultrasmall angle X-ray scattering | 超小角X射線散射 |
UV-Vis | ultraviolet–visible spectroscopy | 紫外可見(jiàn)光譜 |
XPS | X-ray photoemission spectroscopy | X射線光電子能譜�,也稱(chēng)為ESCA |
XRD | X-ray diffraction | X射線衍射 |
XRF | X-ray fluorescence spectrometry | X射線熒光光譜 |
XAFS | X-ray absorption fine structure | X射線吸收精細(xì)結(jié)構(gòu)譜 |
納米物體 | nano-object | 一維、二維或三維外部維度處于納米尺度的物體��。注:用于所有相互分離的納米尺度物體的通用術(shù)語(yǔ)����。(GB/T 30544.1) |
納米顆粒 | nanoparticle | 三個(gè)維度的外部尺寸都在納米尺度的納米物體,其最長(zhǎng)軸和最短軸的長(zhǎng)度沒(méi)有明顯差別���。注:如果納米物體最長(zhǎng)軸和最短軸的長(zhǎng)度差別顯著(大于3倍)時(shí)���,應(yīng)用納米棒、納米纖維或納米片來(lái)表示納米顆粒����。(GB/T 32269-2015) |
納米尺度 | nanoscale | 處于1 nm至100 nm之間的尺寸范圍(GB/T 30544.1) |
納米結(jié)構(gòu)材料 | nanostructure material | 內(nèi)部或表面具有納米結(jié)構(gòu)的材料�����。(GB/T 30544.1) |
六�����、參考文獻(xiàn)
[1]GB/Z 16886.22-2022(ISO/TR 10993.22:2017,IDT),醫(yī)療器械生物學(xué)評(píng)價(jià)-第22部分:納米材料指南[S].
[2]GB/T 39261-2020,納米技術(shù) 納米材料毒理學(xué)評(píng)價(jià)前理化性質(zhì)表征指南[S].
[3]國(guó)家藥品監(jiān)督管理局.醫(yī)療器械注冊(cè)申報(bào)資料要求和批準(zhǔn)證明文件格式:國(guó)家局公告2021年第121號(hào)[Z].
[4]GB/T 38261-2019,納米技術(shù) 生物樣品中銀含量測(cè)量 電感耦合等離子體質(zhì)譜法[S].
[5]ISO/TR 13014:2012,納米技術(shù)——工程納米材料理化特性毒理學(xué)評(píng)估指南Nanotechnologies-Guidance on physico-chemical characterization of engineered nanoscale materials for toxicologic assessment[S].
[6]GB/T 21649.1-2008,粒度分析 圖像分析法 第1部分:靜態(tài)圖像分析法[S].
[7]GB/T 15445.6-2014,粒度分析 結(jié)果的表述 第6部分:顆粒形狀和形態(tài)的定性及定量表述[S].
[8]GB/T 27788-2020,微束分析 掃描電鏡 圖像放大倍率校準(zhǔn)導(dǎo)則[S].
[9]ISO 21363:2020, Nanotechnologies - Measurements of particle size and shape distributions by transmission electron microscopy[S].
[10]ISO 19749:2021, Nanotechnologies - Measurements of particle size and shape distributions by scanning electron microscopy[S].
[11]JY/T 0582-2020,掃描探針顯微鏡分析方法通則[S].
[12]ISO/TS 19590:2019, Nanotechnologies - Size distribution and concentration of inorganic nanoparticles in aqueous media via single particle inductively coupled plasma mass spectrometry[S].
[13]GB/T 29022-2021,粒度分析 動(dòng)態(tài)光散射法(DLS)[S].
[14]GB/T 19627-2005,粒度分析 光子相關(guān)光譜法[S].
[15]GB/T 20307-2006,納米級(jí)長(zhǎng)度的掃描電鏡測(cè)量方法通則[S].
[16]GB/T 30543-2014,納米技術(shù) 單壁碳納米管的透射電子顯微術(shù)表征方法[S].
[17]ISO 19430:2016, Particle size analysis Particle tracking analysis (PTA) method[S].
[18]ISO 13318, Determination of particle size distribution by centrifugal liquid sedimentation methods系列標(biāo)準(zhǔn)[S].
[19]GB/T 19077-2016,粒度分析 激光衍射法[S].
[20]GB/T 32871-2016,單壁碳納米管表征 拉曼光譜法[S].
[21]GB/T 29024,粒度分析 單顆粒的光學(xué)測(cè)量方法 系列標(biāo)準(zhǔn)[S].
[22]GB/T 41316-2022,分散體系穩(wěn)定性表征指導(dǎo)原則[S].
[23]GB/T 38431-2019,顆粒分散體系穩(wěn)定性評(píng)價(jià) 靜態(tài)多重光散射法[S].
[24]GB/T 19587-2017,氣體吸附BET法測(cè)定固態(tài)物質(zhì)比表面積[S].
[25]GB/T 39713-2020,精細(xì)陶瓷粉體比表面積試驗(yàn)方法 氣體吸附BET法[S].
[26]GB/T 21650,壓汞法和氣體吸附法測(cè)定固體材料孔徑分布和孔隙度 系列標(biāo)準(zhǔn)[S].
[27]GB/T 17359-2012,微束分析 能譜法定量分析[S].
[28]GB/T 30703-2014,微束分析 電子背散射衍射取向分析方法導(dǎo)則[S].
[29]GB/T 28634-2012,微束分析 電子探針顯微分析 塊狀試樣波譜法定量點(diǎn)分析[S].
[30]GB/T 25189-2010,微束分析 掃描電鏡能譜儀定量分析參數(shù)的測(cè)定方法[S].
[31]GB/T 30543-2014,納米技術(shù) 單壁碳納米管的透射電子顯微術(shù)表征方法[S].
[32]GB/T 36065-2018,納米技術(shù) 碳納米管無(wú)定形碳����、灰分和揮發(fā)物的分析 熱重法[S].
[33]GB/T 30903-2014,無(wú)機(jī)化工產(chǎn)品 雜質(zhì)元素的測(cè)定 電感耦合等離子體質(zhì)譜法(ICP-MS)[S].
[34]GB/T 38261-2019,納米技術(shù) 生物樣品中銀含量測(cè)量[S].
[35]GB/T 38789-2020,口腔清潔護(hù)理用品 牙膏中10種元素含量的測(cè)定 電感耦合等離子體質(zhì)譜法[S].
[36]GB/T 25185-2010,表面化學(xué)分析 X射線光電子能譜 荷電控制和荷電校正方法的報(bào)告[S].
[37]GB/T 26533-2011,俄歇電子能譜分析方法通則[S].
[38]GB/T 29558-2013,表面化學(xué)分析 俄歇電子能譜 強(qiáng)度標(biāo)的重復(fù)性和一致性[S].
[39]GB/T 29556-2013,表面化學(xué)分析 俄歇電子能譜和X射線光電子能譜 橫向分辨率�、分析面積和分析器所能檢測(cè)到的樣品面積的測(cè)定[S].
[40]GB/T 30702-2014,表面化學(xué)分析 俄歇電子能譜和X射線光電子能譜 實(shí)驗(yàn)測(cè)定的相對(duì)靈敏度因子在均勻材料定量分析中的使用指南[S].
[41]GB/T 28893-2012,表面化學(xué)分析 俄歇電子能譜和X射線光電子能譜 測(cè)定峰強(qiáng)度的方法和報(bào)告結(jié)果所需的信息[S].
[42]GB/Z 32494-2016,表面化學(xué)分析 俄歇電子能譜 化學(xué)信息的解析[S].
[43]GB/T 24581-2022,硅單晶中III、V族雜質(zhì)含量的測(cè)定 低溫傅立葉變換紅外光譜法[S].
[44]GB/T 39114-2020,納米技術(shù) 單壁碳納米管的紫外/可見(jiàn)/近紅外吸收光譜表征方法[S].
[45]JY/T 022-1996,紫外和可見(jiàn)吸收光譜方法通則[S].
[46]GB/T 19502-2004,表面化學(xué)分析 輝光放電發(fā)射光譜方法通則[S].
[47]GB/T 30902-2014,無(wú)機(jī)化工產(chǎn)品 雜質(zhì)元素的測(cè)定 電感耦合等離子體發(fā)射光譜法(ICP-OES)[S].
[48]GB/T 33324-2016,膠乳制品中重金屬含量的測(cè)定 電感耦合等離子體原子發(fā)射光譜法[S].
[49]GB/T 30905-2014,無(wú)機(jī)化工產(chǎn)品 元素含量的測(cè)定 X射線熒光光譜法[S].
[50]JY/T 0573-2020,激光拉曼光譜分析方法通則[S].
[51]GB/T 29858-2013,分子光譜多元校正定量分析通則[S].
[52]JY/T 0578-2020,超導(dǎo)脈沖傅里葉變換核磁共振波譜測(cè)試方法通則[S].
[53]DB46/T 520-2020,全生物降解塑料制品 核磁共振波譜快速檢測(cè)法[S].
[54]GB/T 33523-2017,產(chǎn)品幾何技術(shù)規(guī)范(GPS) 表面結(jié)構(gòu) 區(qū)域法 系列標(biāo)準(zhǔn)[S].
[55]GB/T 33498-2017,表面化學(xué)分析 納米結(jié)構(gòu)材料表征[S].
[56]GB/T 28894-2012,表面化學(xué)分析 分析前樣品的處理[S].
[57]GB/T 40109-2021,表面化學(xué)分析 二次離子質(zhì)譜 硅中硼深度剖析方法[S].
[58]GB/T 25186-2010,表面化學(xué)分析 二次離子質(zhì)譜 - 由離子注入?yún)⒖嘉镔|(zhì)確定相對(duì)靈敏度因子[S].
[59]GB/T 32671,膠體體系 zeta電位測(cè)量方法 系列標(biāo)準(zhǔn)[S].
[60]GB/T 41316-2022,分散體系穩(wěn)定性表征指導(dǎo)原則[S].
[61]GB/T 38431-2019,顆粒 分散體系穩(wěn)定性評(píng)價(jià) 靜態(tài)多重光散射法[S].
[62]歐盟新興與新識(shí)別健康風(fēng)險(xiǎn)委員會(huì)(SCENIHR),醫(yī)療器械中應(yīng)用的納米材料潛在健康效應(yīng)指導(dǎo)原則 Guidance on the Determination of Potential Health Effects of Nanomaterials Used in Medical Devices,Scientific Committee on Emerging and Newly Identified Health Risks[Z]. 2015
[63]THE U.S. FOOD AND DRUG ADMINISTRATION. Nanotechnology—Over a Decade of Progress and Innovation, 2020[R].
[64]G.A.Martínez-Castaón, F.Martínez-Gutiérrez, F.Ruiz, et al. Characterization and biocompatibility of chitosan gels with silver and gold nanoparticles[J]. J Nanomater, 2014, 543419.
[65]Harada Masafumi, Yamamoto Miho, Iwase Hiroki. Combined small-angle neutron scattering/small-angle X?ray scattering analysis for the characterization of silver nanoparticles prepared via photoreduction in water-in-oil microemulsions[J]. Langmuir 2021, 37:13085?13098.
[66]J Liu���,KE Murphy��,RI Maccuspie, et al. Capabilities of single particle inductively coupled plasma mass spectrometry for the size measurement of nanoparticles: a case study on gold nanoparticles[J]. Anal. Chem. 2014, 86:3405–3414.
[67]DE Gorka, NJ Lin, JM Pettibone, et al. Chemical and physical transformations of silver nanomaterial containing textiles after modeled human exposure[J]. NanoImpact. 2019, 14C:100160.
[68]Wang Liming, Zhang Tianlu Li Panyun, et al. Use of Synchrotron Radiation-Analytical Techniques To Reveal Chemical Origin of Silver-Nanoparticle Cytotoxicity[J]. ACS Nano 2015, 9:6532-6547.
[69]YY/T 1295-2015,醫(yī)療器械生物學(xué)評(píng)價(jià) 納米材料:細(xì)菌內(nèi)毒素試驗(yàn)[S].
[70]YY/T 0993-2015,醫(yī)療器械生物學(xué)評(píng)價(jià) 納米材料:體外細(xì)胞毒性試驗(yàn)(MTT試驗(yàn)和LDH試驗(yàn))[S].
[71]YY/T 1532-2017,醫(yī)療器械生物學(xué)評(píng)價(jià) 納米材料 溶血試驗(yàn)[S].
[72]YY/T 1863-2023,納米醫(yī)療器械生物學(xué)評(píng)價(jià) 含納米銀敷料中銀顆粒和銀離子的釋放與表征方法[S].
七���、編寫(xiě)單位
本指導(dǎo)原則由國(guó)家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評(píng)中心牽頭,國(guó)家納米科學(xué)中心���、中國(guó)食品藥品檢定研究院參與編寫(xiě)�,由國(guó)家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評(píng)中心負(fù)責(zé)解釋��。