蒙古國衛(wèi)生部藥品和醫(yī)療器械司負(fù)責(zé)診斷藥品和醫(yī)療器械注冊(cè)和審查工作,蒙古醫(yī)療器械注冊(cè)的法規(guī)依據(jù)是蒙古國政府于2010 年6月1日發(fā)布的《藥品和醫(yī)療器械法》�。
蒙古國衛(wèi)生部藥品和醫(yī)療器械司負(fù)責(zé)診斷藥品和醫(yī)療器械注冊(cè)和審查工作,蒙古醫(yī)療器械注冊(cè)的法規(guī)依據(jù)是蒙古國政府于2010 年6月1日發(fā)布的《藥品和醫(yī)療器械法》����。

一、蒙古國醫(yī)療器械注冊(cè)模式
不同于我國對(duì)醫(yī)療器械注冊(cè)審批流程���,醫(yī)療產(chǎn)品和醫(yī)療設(shè)備不需要在蒙古注冊(cè)����。采購機(jī)構(gòu)進(jìn)出口藥品����、醫(yī)療器械,應(yīng)當(dāng)取得《藥品����、醫(yī)療器械進(jìn)口許可證》����。進(jìn)口許可證應(yīng)當(dāng)載明藥品�、醫(yī)療器械的名稱、種類���、劑量��、數(shù)量���、生產(chǎn)企業(yè)名稱、國境口岸和日期�。
診斷工具包(Diagnostic Kits)必須根據(jù)蒙古衛(wèi)生部2019年9月9日第A295號(hào)命令“關(guān)于批準(zhǔn)藥品和物質(zhì)注冊(cè)條例”。診斷用醫(yī)療產(chǎn)品的注冊(cè)程序類似于藥品的注冊(cè)程序��。
二�����、蒙古醫(yī)療器械注冊(cè)申請(qǐng)條件
進(jìn)口藥品���、生物修復(fù)、藥用原料和醫(yī)療器械(以下簡稱“進(jìn)口藥品和醫(yī)療器械”)的組織必須符合下列基本要求����。
A) 必須有儲(chǔ)存藥品和醫(yī)療設(shè)備的倉庫;
B) 必須有一名從有執(zhí)照提供醫(yī)學(xué)教育的學(xué)校畢業(yè)的醫(yī)務(wù)專業(yè)人員��,他將從事藥品和醫(yī)療器械的質(zhì)量認(rèn)證���、儲(chǔ)存和分發(fā)活動(dòng);
C) 進(jìn)口藥品必須在國家藥品注冊(cè)中心注冊(cè);而且
D) 醫(yī)療器械必須有技術(shù)質(zhì)量認(rèn)證文件,藥用原料必須符合質(zhì)量要求�����。進(jìn)口藥品�、醫(yī)療器械許可證的有效期不得超過1年。出口藥品和醫(yī)療器械藥品�����、生物修復(fù)����、藥用原料和醫(yī)療器械的出口和轉(zhuǎn)口許可證由藥品、生物修復(fù)和治療質(zhì)量控制辦公室在人類醫(yī)藥部門理事會(huì)的評(píng)估基礎(chǔ)上頒發(fā)�����。
三、蒙古國醫(yī)療器械注冊(cè)審批流程
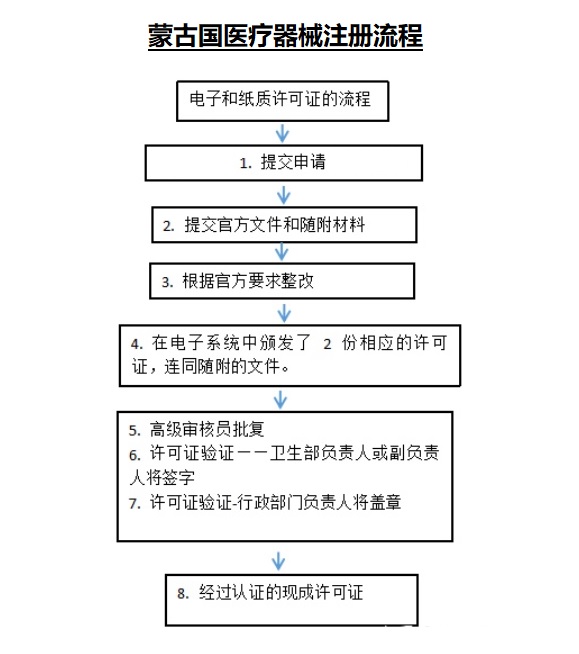
在進(jìn)口許可證申請(qǐng)中�����,應(yīng)當(dāng)附有下列文件��。
2.2.1. 與該藥品或醫(yī)療器械的制造商�����、出口機(jī)構(gòu)或持牌經(jīng)銷商簽訂的銷售合同�����;
2.2.2. 合同規(guī)定進(jìn)口貨物的發(fā)票�����;
2.2.3. 在進(jìn)口醫(yī)療器械時(shí)�,應(yīng)提供保證滿足國際標(biāo)準(zhǔn)組織(ISO)的制造商和產(chǎn)品要求的證書。
更多有關(guān)蒙古國醫(yī)療器械注冊(cè)服務(wù)需求����,歡迎您隨時(shí)方便與杭州證標(biāo)客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡(luò),聯(lián)系人:葉工�,電話:18058734169����,微信同����。