2023年8月29日,為及時(shí)研究并解決GB 9706.1-2020及配套并列標(biāo)準(zhǔn)�、專用標(biāo)準(zhǔn)實(shí)施的重大技術(shù)問題,更好地發(fā)揮技術(shù)支撐作用���,國家藥品監(jiān)督管理局醫(yī)療器械標(biāo)準(zhǔn)管理中心根據(jù)《國家藥品監(jiān)督管理局關(guān)于GB 9706.1-2020及配套并列標(biāo)準(zhǔn)�����、專用標(biāo)準(zhǔn)實(shí)施有關(guān)工作的通告》有關(guān)要求���,制定并發(fā)布了《GB 9706.1-2020及配套并列標(biāo)準(zhǔn)��、專用標(biāo)準(zhǔn)專家咨詢機(jī)制》�,詳見正文。
2023年8月29日���,為及時(shí)研究并解決GB 9706.1-2020及配套并列標(biāo)準(zhǔn)��、專用標(biāo)準(zhǔn)實(shí)施的重大技術(shù)問題���,更好地發(fā)揮技術(shù)支撐作用,國家藥品監(jiān)督管理局醫(yī)療器械標(biāo)準(zhǔn)管理中心根據(jù)《國家藥品監(jiān)督管理局關(guān)于GB 9706.1-2020及配套并列標(biāo)準(zhǔn)����、專用標(biāo)準(zhǔn)實(shí)施有關(guān)工作的通告》有關(guān)要求,制定并發(fā)布了《GB 9706.1-2020及配套并列標(biāo)準(zhǔn)、專用標(biāo)準(zhǔn)專家咨詢機(jī)制》����,詳見正文。
GB 9706.1-2020及配套并列標(biāo)準(zhǔn)�����、專用標(biāo)準(zhǔn)專家咨詢機(jī)制
為及時(shí)研究并解決GB 9706.1-2020 及配套并列標(biāo)準(zhǔn)���、專用標(biāo)準(zhǔn)實(shí)施的重大技術(shù)問題��,更好地發(fā)揮技術(shù)支撐作用����,統(tǒng)一對(duì)標(biāo)準(zhǔn)的理解和認(rèn)識(shí)��,規(guī)范執(zhí)行尺度�,推進(jìn)標(biāo)準(zhǔn)順利實(shí)施,特制定本機(jī)制��。
一�����、受理范圍
GB 9706.1-2020及配套并列標(biāo)準(zhǔn)、專用標(biāo)準(zhǔn)實(shí)施過程中���,藥品監(jiān)督管理部門�����、技術(shù)審查部門�����、醫(yī)療器械檢驗(yàn)機(jī)構(gòu)對(duì)標(biāo)準(zhǔn)內(nèi)容理解存在差異等影響標(biāo)準(zhǔn)實(shí)施的重大技術(shù)問題���。
二�����、專家組成員單位
牽頭單位:中國食品藥品檢定研究院(國家藥品監(jiān)督管理局醫(yī)療器械標(biāo)準(zhǔn)管理中心)(以下簡稱器械標(biāo)管中心)�。
成員單位:中國食品藥品檢定研究院、國家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評(píng)中心����、相關(guān)標(biāo)準(zhǔn)歸口醫(yī)療器械標(biāo)準(zhǔn)化技術(shù)委員會(huì)。
根據(jù)咨詢所涉標(biāo)準(zhǔn)情況�����,可增加有代表性產(chǎn)品的屬地藥品監(jiān)督管理部門以及屬地藥品監(jiān)督管理部門醫(yī)療器械技術(shù)審查部門、具有相關(guān)檢驗(yàn)資質(zhì)的醫(yī)療器械檢驗(yàn)機(jī)構(gòu)����。
三、工作程序
(一)省級(jí)藥品監(jiān)督管理部門�����、技術(shù)審查部門��、醫(yī)療器械檢驗(yàn)機(jī)構(gòu)之間若對(duì)標(biāo)準(zhǔn)內(nèi)容理解存在差異等影響標(biāo)準(zhǔn)實(shí)施的重大技術(shù)問題且無法協(xié)調(diào)一致的可書面向器械標(biāo)管中心提交咨詢(提交內(nèi)容和要求見附1)���。
(二)器械標(biāo)管中心根據(jù)咨詢事項(xiàng)涉及的標(biāo)準(zhǔn)��,組織標(biāo)準(zhǔn)歸口的醫(yī)療器械標(biāo)準(zhǔn)化技術(shù)委員會(huì)開展研究�����。技術(shù)委員會(huì)應(yīng)及時(shí)和提出單位進(jìn)行充分溝通���,原則上應(yīng)在15個(gè)工作日內(nèi)提出處理意見。若能形成一致意見��,由技術(shù)委員會(huì)對(duì)相關(guān)問題予以書面解答,視情況發(fā)布相關(guān)解釋性文件���,并將相關(guān)情況報(bào)送器械標(biāo)管中心;若不能達(dá)成一致���,技術(shù)委員會(huì)提出處理意見、報(bào)器械標(biāo)管中心研究�����,是否啟動(dòng)專家咨詢����。
(三)若啟動(dòng)專家咨詢,器械標(biāo)管中心將視情況組織咨詢會(huì)議,由專家組成員單位根據(jù)咨詢事項(xiàng)推薦1名專家代表本單位參加會(huì)議��。
(四)會(huì)議由器械標(biāo)管中心主持�,如需要�,器械標(biāo)管中心可于會(huì)議開始前指定專家組組長。會(huì)議原則上協(xié)商一致�����,提出解決方案�,形成專家會(huì)商意見����。若不能達(dá)成一致�����,進(jìn)行投票表決�����,超過半數(shù)的意見作為專家會(huì)商意見����。.
(五)對(duì)影響標(biāo)準(zhǔn)全面實(shí)施的整體性、共性問題���,器械標(biāo)管中心在專家會(huì)商意見的基礎(chǔ)上�����,組織起草解釋性文件����。國家標(biāo)準(zhǔn)的解釋報(bào)送國務(wù)院標(biāo)準(zhǔn)化行政主管部門發(fā)布;行業(yè)標(biāo)準(zhǔn)的解釋由國家藥品監(jiān)督管理局發(fā)布�����。
四、附則
(一)本機(jī)制由器械標(biāo)管中心負(fù)貴解釋��。
(二)本機(jī)制自發(fā)布之日起實(shí)施��。
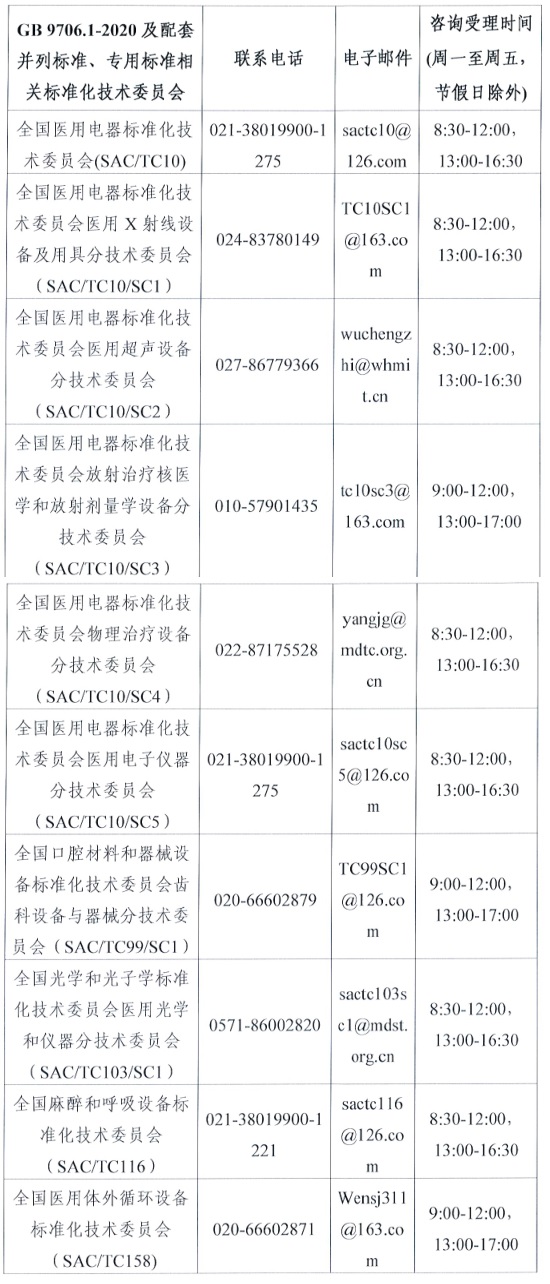
(三)關(guān)于GB 9706.1-2020 及配套并列標(biāo)準(zhǔn)��、專用標(biāo)準(zhǔn)的具體技術(shù)問題�����,可電話咨詢所涉標(biāo)準(zhǔn)歸口的醫(yī)療器械標(biāo)準(zhǔn)化技術(shù)委員會(huì)�����,聯(lián)系電話見附2���。
附件1.GB9706.1-2020及配套并列標(biāo)準(zhǔn)�����、專用標(biāo)準(zhǔn)專家咨詢事項(xiàng)信息表

附件2.GB9706.1-2020及配套并列標(biāo)準(zhǔn)���、專用標(biāo)準(zhǔn)相關(guān)標(biāo)準(zhǔn)化技術(shù)委員會(huì)
更多有關(guān)GB9706.1-2020標(biāo)準(zhǔn)��、可用性工程文檔編制服務(wù)等需求����,歡迎您隨時(shí)方便與杭州證標(biāo)客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡(luò),聯(lián)系人:葉工�����,電話:18058734169����,微信同。