醫(yī)療器械臨床試驗、體外診斷試劑臨床試驗法規(guī)及監(jiān)管制度來源于藥品臨床試驗法規(guī)���,但是由于產(chǎn)品的特性及風(fēng)險差異較大�,醫(yī)療器械臨床試驗法規(guī)與藥品���、體外診斷試劑臨床試驗法規(guī)又存在較大差異���,我們一起來看一下。
引言:醫(yī)療器械臨床試驗���、體外診斷試劑臨床試驗法規(guī)及監(jiān)管制度來源于藥品臨床試驗法規(guī),但是由于產(chǎn)品的特性及風(fēng)險差異較大���,醫(yī)療器械臨床試驗法規(guī)與藥品�����、體外診斷試劑臨床試驗法規(guī)又存在較大差異���,我們一起來看一下�����。
一���、藥品、體外診斷試劑�、醫(yī)療器械臨床試驗法規(guī)見下圖:
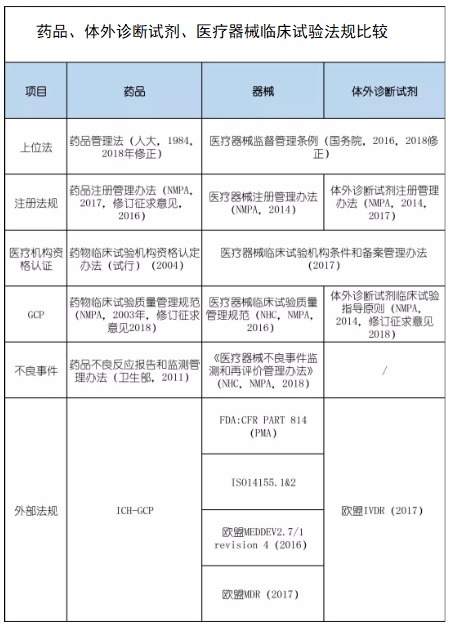
二、醫(yī)療器械臨床試驗法規(guī)與藥品����、體外診斷試劑法規(guī)的差異說明:
1、首先�����,我們看到,醫(yī)療器械臨床試驗法規(guī)與體外診斷試劑在國內(nèi)基本一致�,在國外則存在差異。
2����、醫(yī)療器械臨床試驗質(zhì)量管理規(guī)范及體外診斷試劑臨床試驗指導(dǎo)原則來源于藥物臨床試驗管理規(guī)范,但與其又存在較大差異�����,特別是在臨床試驗分期方面�。
3、不良事件層面���,主要是報告對象及事故處理方面存在較大差異�。
4�、注冊法規(guī)層面,藥品與醫(yī)療器械����、體外診斷試劑存在較大差異,醫(yī)療器械與體外診斷試劑基本一致�����。