對(duì)于在醫(yī)療器械注冊(cè)進(jìn)程中,臨床試驗(yàn)前����,醫(yī)療器械產(chǎn)品是否需要做動(dòng)物實(shí)驗(yàn)對(duì)很多行業(yè)從業(yè)者都是一個(gè)問(wèn)題,今年初�,國(guó)家藥品監(jiān)督管理局組織制定了《醫(yī)療器械動(dòng)物實(shí)驗(yàn)研究技術(shù)審查指導(dǎo)原則 第一部分:決策原則》,為企業(yè)提供了是否需要做動(dòng)物實(shí)驗(yàn)決策的法規(guī)依據(jù)���。
引言:對(duì)于在醫(yī)療器械注冊(cè)進(jìn)程中�,臨床試驗(yàn)前�����,醫(yī)療器械產(chǎn)品是否需要做動(dòng)物實(shí)驗(yàn)對(duì)很多行業(yè)從業(yè)者都是一個(gè)問(wèn)題��,今年初��,國(guó)家藥品監(jiān)督管理局組織制定了《醫(yī)療器械動(dòng)物實(shí)驗(yàn)研究技術(shù)審查指導(dǎo)原則 第一部分:決策原則》���,為企業(yè)提供了是否需要做動(dòng)物實(shí)驗(yàn)決策的法規(guī)依據(jù)。
一���、醫(yī)療器械注冊(cè)是否需要做動(dòng)物實(shí)驗(yàn)的法規(guī)依據(jù):
2019年4月18日��,國(guó)家藥監(jiān)局為加強(qiáng)醫(yī)療器械產(chǎn)品注冊(cè)工作的監(jiān)督和指導(dǎo)��,進(jìn)一步提高注冊(cè)審查質(zhì)量����,國(guó)家藥品監(jiān)督管理局組織制定了《醫(yī)療器械動(dòng)物實(shí)驗(yàn)研究技術(shù)審查指導(dǎo)原則 第一部分:決策原則》,為企業(yè)和審評(píng)人員�����、監(jiān)管人員判定醫(yī)療器械注冊(cè)過(guò)程中是否需要做動(dòng)物實(shí)驗(yàn)提供了法規(guī)依據(jù)����。
二、醫(yī)療器械注冊(cè)過(guò)程中可能需要做動(dòng)物實(shí)驗(yàn)的產(chǎn)品舉例:
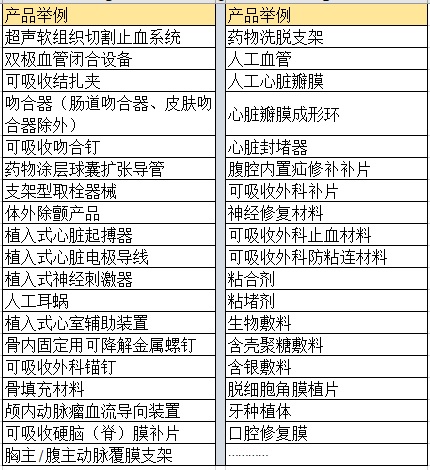
杭州證標(biāo)客醫(yī)藥技術(shù)咨詢有限公司位于中國(guó)杭州�����,是醫(yī)療器械專(zhuān)業(yè)服務(wù)第三方�。為廣大客戶提供醫(yī)療器械法律法規(guī)、經(jīng)營(yíng)開(kāi)辦��、醫(yī)療器械生產(chǎn)質(zhì)量管理體系���、醫(yī)療器械注冊(cè)�����、臨床����、CRC、CE���、FDA���、醫(yī)療信息系統(tǒng)定制開(kāi)發(fā)一站式服務(wù),是江浙滬地區(qū)極少數(shù)有醫(yī)療器械全流程服務(wù)能力的機(jī)構(gòu)之一����。任何有關(guān)醫(yī)療器械注冊(cè)��、醫(yī)療器械經(jīng)營(yíng)許可/備案�����、醫(yī)療器械臨床試驗(yàn)����、CRC服務(wù)事宜,隨時(shí)方便聯(lián)系葉工(MP:18058734169,微信同)��。